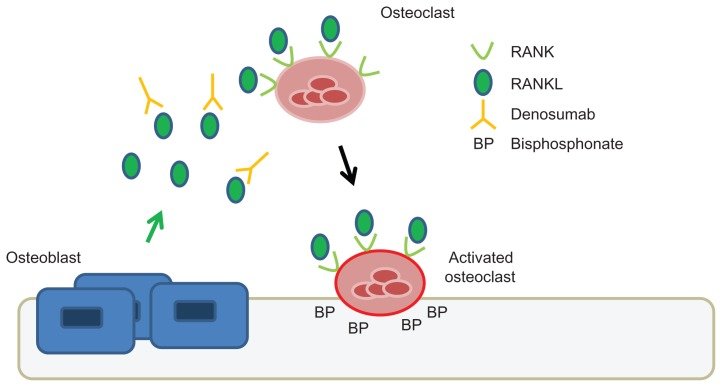
Ernährung bei Prolia/Denosumab - Das sollten Sie für eine effektive Therapie beachten.
Das Medikament Denosumab, Handelsname Prolia, wird häufig in der Behandlung von Osteoporose eingesetzt. In diesem Artikel erfahren Sie wie der moderne Wirkstoff den Knochenschwund behandeln kann, wie effektiv die Therapie ist und was Neben- und Wechselwirkungen sind. Zudem wird auf die Ernährung und deren Rolle in der Effizienz und Vermeidung von Nebenwirkungen eingegangen.